- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体的提取方法:1、磁珠免疫法。外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。2、多聚物沉淀法。聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集病毒,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等由于这些核酸被囊膜包裹而被保护,稳定性高,不易降解。贵阳正规外泌体提取试剂供应商

密度梯度离心法该方法由于比较繁琐,用的较少。原理是:像所有的脂质小囊泡一样,外泌体可以悬浮于特定密度梯度的蔗糖中,其密度范围1.13g/ml-1.21g/ml,将要分离外泌体的样本液体置于梯度蔗糖介质上,随后通过离心将外泌体分离。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感。具体步骤是:收集培养2d的上清液。将培养上清液先以1500r/min离心5min除去细胞及碎片,再依次以1000×g离心10min取上清,10000×g离心30min取上清,然后用100ku超滤离心管(Millipore)浓缩至15mL,厦门正规外泌体提取试剂供应商专利申请利用分离培养人尿液来源细胞并收集培养基来进行体外培养。
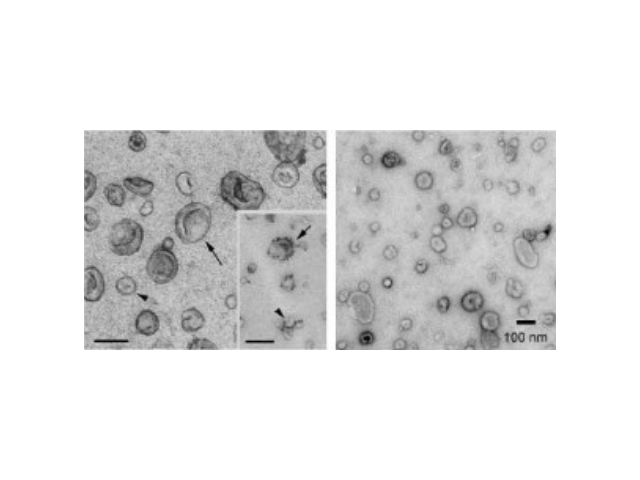
大量关于一些病症相关巨噬细胞的研究表明,一些病症相关巨噬细胞通过与一些病症细胞进行细胞间通讯,与一些病症进展和转移相关,然而对TAM与一些病症细胞之间通信的研究限制于可溶性因子,例如促炎细胞因子,其中包括趋化因子、炎症因子和生长因子等。较近的研究证据表明,外泌体是一些病症微环境中不同细胞类型之间的重要通讯媒介。外泌体将信息从一个细胞传递到另一个细胞并重编程受体细胞。目前大部分研究都集中在一些病症细胞分泌的外泌体,关于TAM衍生的外泌体及其对治病细胞的影响知之甚少。TAM具有两种相反的表型:M1亚型巨噬细胞具有抗一些病症作用,M2型巨噬细胞具有致瘤作用活性。TAM的表型由特定的一些病症来源的趋化因子和外泌体调节。较近的一项研究表明,一些病症来源的外泌体miRNA调节一些病症促进M2巨噬细胞的极化。然而,TAM衍生的外泌体对一些病症进展和转移的调节尚未明确定义。目前,TAM的外泌体概况仍然大部分未知,并且TAM衍生的外泌体对于一些病症进展在功能上是否必需还未确定。
来源于不同的组织的外泌体不仅具有其特异性蛋白分子,而且还包含其行使功能的关键分子。有关外泌体分泌和摄取及其组成、“运载物”和相应功能的精确分子机制近些年刚刚开始受到关注,与外泌体相关的被pubmed收录的文章数量和国自然基金项目中标数量逐年增长,表明国内外对外泌体的研究兴趣日益增长。细胞外囊泡是蛋白质、mRNA、miRNA和脂质运输来完成细胞间通讯通路的重要媒介,根据它们的大小和发生分为三类,包括外泌体、微泡和凋亡小体。其中,外泌体是直径大约为40-100nm的包装囊泡,由多种细胞分泌,内含有特定的蛋白质、脂质、细胞因子或遗传物质。近几年来,市场上已出现各种商业化的外泌体提取试剂盒。

外泌体相关miRNA与肺病的诊断:miRNAs是一类含有20~25个核苷酸的非编码小RNA,能够通过下调或压制靶mRNAs来调节转录水平上的基因表达,目前非编码RNA被普遍发现存在于NSCLC患者外泌体中,参与一些病症的形成和演化过程。单个miRNA可能通过压制性复合物与多个mRNA结合,从而阻滞整个生物通路。因此,外泌体的miRNA具有成为NSCLC标志物的优势。Chen等在152例肺病患者的研究中初次报道了循环游离miRNA的表达,与75例健康者相比,发现了两种高表达的miRNA(miR-25和miR-223)。Rabinonowits等对27例肺病患者和9例健康人的血浆外泌体中12个miRNA的表达进行了评估,结果显示,12个一些病症相关的miRNA*在肺病患者中过度表达。Cazzoli等收集了30个血浆样本,发现4种外泌体miRNA(miR-378a、-379a、-139-5p、-200b-5p)在肺病患者血清中明显升高,用于筛查患者与健康人ROC曲线下面积(AUC)为0.908。聚乙二醇(PEG)可与疏水性蛋白和脂质分子结合共沉淀。外泌体提取试剂厂家直销
外泌体的提取分离:密度梯度离心。贵阳正规外泌体提取试剂供应商
外泌体的提取方法,先用含无外泌体血清的培养基对人脂肪来源间充质干细胞进行饥饿培养,这样可使干细胞处于正常生长状态,不会被克制生长增殖,其所分泌的外泌体所包含的有效物质也更贴近其自然状态下的外泌体,然后将含有外泌体的培养上清液进行低速差速离心(即先一离心处理、再第二离心处理)以去除细胞及其碎片,用100kd超滤管对低速差速离心后的离心液进行超滤浓缩得到外泌体浓度更高的超滤液,将超滤液经过第三离心处理去除杂质后直接用0.22μm过滤器过滤除菌,过滤掉粒径为220nm以上的物质,进一步得到含颗粒粒径小于220nm的浓缩液,因超滤浓缩处理和第三离心处理使得液体量浓缩,这样过滤除菌效率得到较大提高,较后将浓缩液进行超速离心的第四离心处理分离提取到外泌体。该外泌体的提取方法,既结合了差速离心,又结合了超滤和超速离心,通过该提取流程,较终可高效地从人脂肪来源间充质干细培养上清液中提取到高浓度、高纯度的外泌体,具有操作简单、成本低,适合产业化生产的特点。贵阳正规外泌体提取试剂供应商
外泌体的提取方法学规范、统一定量及鉴定等。关于外泌体的提取有超速离心、试剂盒、超滤法、蔗糖密度梯度离心等,然而各种方法均有其利弊。超速离心法是目前外泌体相关文章中的主流方法,由于离心步骤繁琐,费事费力,而且步骤多导致实验中容易污染,且损耗量大,使得较终回收的外泌体不稳定。而且对于抽提细胞上清来说,更是极为不请便,试想用提取300ml的上清需要6个50ml离心管,无论是过滤还是后续的每一步的离心去沉淀,都具有操作极其不便的缺点,总之非常麻烦。而超滤法存在外泌体会堵塞膜孔,造成浓缩效率低,浓缩管重复利用差,甚至堵塞在膜孔的外泌体还可能会粘连成团,造成损失及较后的数据有误差,对于后续实验也有影响无法...
- 温州正规外泌体提取试剂报价 2024-11-14
- 温州正规外泌体提取试剂销售厂家 2024-11-13
- 南京正规外泌体提取试剂服务电话 2024-11-13
- 上海外泌体提取试剂哪家好 2024-11-13
- 深圳外泌体提取试剂哪家便宜 2024-11-13
- 重庆外泌体提取试剂厂家批发价 2024-11-13
- 重庆外泌体提取试剂哪家好 2024-11-13
- 珠海外泌体提取试剂产品介绍 2024-11-13
- 杭州外泌体提取试剂哪家好 2024-11-13
- 郑州外泌体提取试剂哪家好 2024-11-13
- 南京外泌体提取试剂哪家便宜 2024-11-11
- 杭州正规外泌体提取试剂厂家批发价 2024-11-11
- 广州正规外泌体提取试剂报价 2024-11-11
- 徐州正规外泌体提取试剂报价 2024-11-11
- 昆明正规外泌体提取试剂厂家直销 2024-11-11
- 芜湖外泌体提取试剂报价 2024-11-11


- 济南RNA提取试剂平均价格 11-22
- 重庆RNA提取试剂生产厂家 11-22
- 昆明正规RNA提取试剂厂家直销 11-22
- 广州RNA提取试剂厂家直销 11-22
- 开封RNA提取试剂哪家好 11-22
- 天津正规RNA提取试剂厂家现货 11-22
- 厦门RNA提取试剂厂家供应 11-22
- 厦门正规RNA提取试剂直销厂家 11-22
- 杭州RNA提取试剂价格 11-22
- 青岛正规RNA提取试剂哪家好 11-22