动物心梗模型中,研究人员通常会采用手术或药物手段来阻塞动物的冠状动脉,以模拟人类心梗的发生。这种阻塞会导致心肌缺血,进而引发心肌梗死。通过对动物模型的观察和研究,研究人员可以了解心肌梗死的病理生理变化,包括心肌细胞的坏死、炎症反应以及心脏功能的改变等。 此外,动物心梗模型还可以用于评估新的治*策略和药物的效果。研究人员可以通过对动物模型的治*,观察其心肌梗死范围、心肌功能以及生存率等指标的变化,从而判断治*策略或药物的疗效。 总之,动物心梗模型研究为我们提供了研究心肌梗死发病机制和治*策略的重要工具,有助于我们更好地理解这种严重疾病的本质,并为开发新的治*方法提供实验依据。为了推动心梗治*研究的发展,需要加强研究规范化工作。上海大小鼠心肌梗死(MI)模型周期短

目前建立心肌梗死动物模型的方法有多种,包括:冠脉结扎法、药物法、球囊堵闭法、栓塞法以及血栓形成法等。冠状动脉结扎法操作简单、血管阻塞明确,比较符合心梗发生的病理过程,能较好的实现临床转化。建立疾病的实验动物模型常常是研究工作至关重要的一步,需要考虑多方面的因素,使疾病本身特征和研究目的与所建立的动物模型达到尽可能地一致。目前心梗治*研究不断深入,基于心肌细胞不可再生的特性,移植治*、干细胞治*、基因治*等多种治*手段及相关机制研究成为心梗治*方案的新方向,建立一种稳定性强、成功率高的小鼠心梗模型是非常必要的。 上海大小鼠心肌梗死(MI)模型周期短这种模型有助于研究心梗的发病机制,并寻找新的治*策略。

在心梗术后的评估中,肢体导联心电图扮演着重要的角色。通过心电图的监测,可以及时发现并评估心肌梗死后心脏电生理的变化。 在实验中,我们采用了异氟烷吸入麻醉的实验鼠,并固定其仰卧位。然后,我们连接了心脏导联线,并将针电极分别固定在右上肢、左上肢和右下肢。为了确保心电图的准确性,我们还特别注意避免了周围磁场的干扰。 在基线平稳后,我们记录了4-5个心动周期的心电图数据。根据心电图的ST段变化,我们发现当ST段弓背向上抬高并持续15分钟以上时,这被作为评判心肌梗死造模成功的标志。 肢体导联心电图在心梗术后的评估中具有重要意义。它可以帮助我们及时发现心脏电生理的变化,为临床医生提供有价值的参考信息,从而更好地指导治*和预后评估。
小鼠心梗模型还可以用于评估新的治*方法和药物的效果。在实验室中,研究人员可以通过对小鼠实施不同的治*方法或药物治*,观察其对心梗的疗效和安全性。这种模型可以帮助我们筛选出有效的治*方法和药物,为临床试验提供实验依据。 同时,小鼠心梗模型还可以用于研究心梗对心脏功能的影响。心梗会导致心脏功能下降,包括心肌收缩力减弱、心律失常等。通过小鼠心梗模型,我们可以观察到心梗对心脏功能的影响,并研究如何保护心脏功能,为临床治*提供指导。 总之,小鼠心梗模型在心梗研究中具有重要作用。它可以帮助我们深入了解心梗的发病机制,评估新的治*方法和药物的效果,以及研究心梗对心脏功能的影响。这种模型的多样性和灵活性使得它成为心梗研究中的一种重要工具。在建立心肌梗死动物模型时,需要综合考虑多方面的因素。
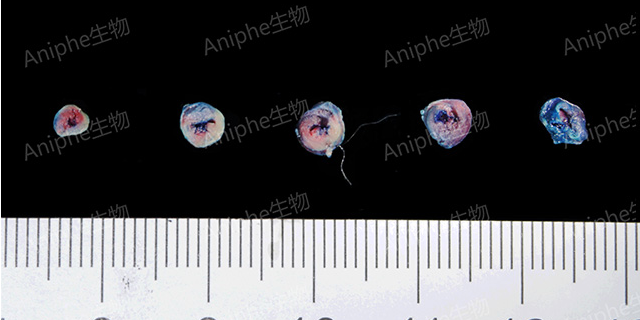
动物处死前,实验鼠麻醉后仰卧位固定,彻底暴露胸腔,将0.5%伊文斯蓝溶液经心尖部注入心腔,完毕后迅速取出心脏,反复用预冷的0.9%氯化钠溶液进行冲洗并剪除残留包膜及血管,用滤纸吸干水分。全心室心脏标本置于–20℃冷冻约30min后取出,在结扎线水平下将将左心室部分垂直长轴切成2-3mm的横断片,浸入2%TTC磷酸缓冲液中,置入37℃水浴反应30分钟。用4%的甲醛固定24h,以增强染色颜色对比,对切片进行扫描拍照。正常心肌染成蓝色,缺血心肌染成砖红色,梗死心肌不着色。小鼠和人类有着相似的遗传物质,这意味着小鼠心梗模型可以更好地模拟人类心梗的遗传背景。上海大小鼠心肌梗死(MI)模型周期短
TTC染色后,梗死区呈现白色,梗死边缘区为砖红色,正常区为红色。上海大小鼠心肌梗死(MI)模型周期短
小鼠心梗模型的优势主要包括以下几个方面: 1. 遗传背景一致:小鼠的遗传背景相对一致,可以减少实验误差,提高实验的可重复性。 2. 操作简便:小鼠体型小,操作相对简便,便于实验操作和观察。 3. 成本较低:小鼠模型相对于其他大型动物模型成本更低,可以节约实验成本。 4. 易于建立稳定的疾病模型:小鼠模型可以较容易地建立稳定的疾病模型,如心肌梗死模型,便于进行后续的疾病研究。 综上所述,小鼠心梗模型具有遗传背景一致、操作简便、成本较低、易于建立稳定的疾病模型等优势。上海大小鼠心肌梗死(MI)模型周期短