eCTD生命周期管理与变更提交:欧盟要求eCTD申报资料覆盖yao品全生命周期,包括提交、补充申请及实质性变更。例如,增成员国需提交“附加成员国序列”,审评时间约52-83天;重大变更(如生产工艺调整)需创建序列并通过CTIS平台更模块3和模块1的GMP证明。技术验证工具(如EDQM推荐的检查软件)需在每次提交前运行,确保XML骨架文件与PDF书签层级符合规范。此外,电子签章需符合《欧盟电子签名法》,并在模块1中明确标注法律效力。欧洲通用提交门户(CommonEuropeanSubmissionPortal,CESP)是欧盟及成员国yao品监管机构间用于电子化提交申报资料的重要平台。以下是关于CESP的详细介绍:CESP是由欧盟yao品监管部门负责人网络(HMA)合作开发的在线交付系统,旨在为yao品注册申请者、利益相关方和监管机构之间提供统一、安全的电子提交通道。其设计初衷是简化跨国申报流程,允许通过单一门户向多个欧洲guo家的yao监部门同时提交申请,避免了重复操作。 eCTD申报相关技术支持。安徽CDE eCTD服务放心可靠
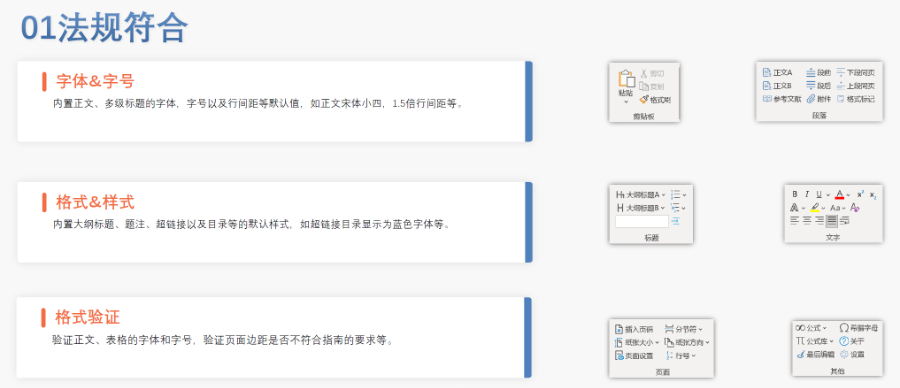
ANDA一般不需要提供临床前(动物)和临床(人体)数据来证明其安全性和youxiao性(即免毒理和临床),作为替代,申请人必须合理证明其产品与原研YAO相比是shengwu等效的。按照《联邦食品、YAO品和化妆品法》第505(j)章要求,拟向FDA递交申请ANDA的YAO品需符合以下条件:仿制YAO必须依照FDA《经过yiliao等同性评价批准的YAO品》(俗称"橙皮书")上所列,由FDA选定的RLD/RS进行对照仿制;活性成份、剂型、规格、给YAO途径、适应症,要与RLD相同;仿制YAO必须证明与RLD在shengwu效果上等同,即具有shengwu等效性;必须按照美国联邦管理法21CFR遵行YAO品生产管理规范kongzhi生产过程;无论CN还是美国,要求仿制YAO的质量必须等同或者是高于参比制剂的,这是获批的基本要点;注意:如果原研YAO未被列为RLD,申请人可以提出公民,向FDA申请。芜湖国产eCTD哪家好欧盟eCTD验证标准相关技术支持。
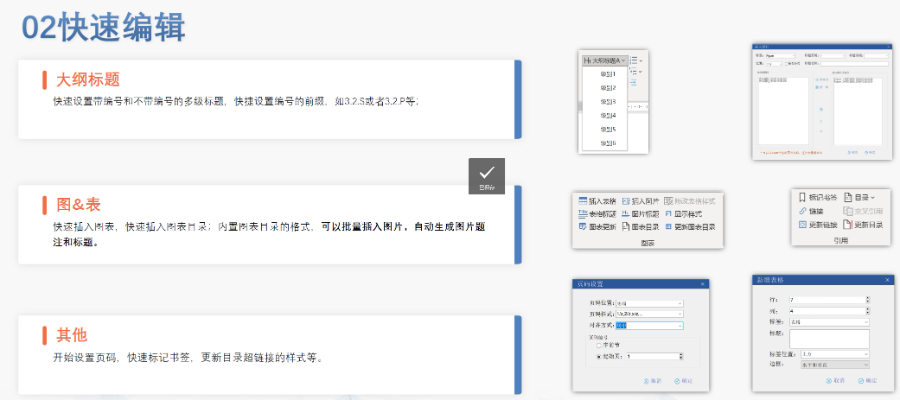
ANDA递交:按照ICHM4的CTD格式整理资料,并以eCTD格式递交;通过ESG通道递交资料;收到CDER的letter,说明资料已经进入FDA数据库;付GDUFA费,在资料递交后的10日内到账;ANDA接收:缴费后,FDA初步审查资料的完整性,并会在60天给答复。第一种情况是ANDA无缺陷,FDA给申请人发受理信(AcceptanceLetter);第二种情况是ANDA包含少于10个小缺陷,FDA将会通过电话、传真、电子邮件等方式通知发布IR(信息请求函),让申请人在7个日历日内改正,若未按时补充所有需要的资料,FDA将拒收该ANDA;第三种情况是ANDA包含1个或者多个重大缺陷,或10个以上的小缺陷,FDA将拒收该ANDA;注:如果这边被拒收,只退75%的费用。
赋悦eCTD系统文件验证与修复支持自动验证文件格式(如PDF属性、字体嵌入、超链接完整性等),并一键修复不符合法规要求的文件。例如,系统会自动检查XML主干文件的结构合规性,确保符合zhong国、美国、欧盟等地区的eCTD法规标准。eCTD组装与发布可自动生成符合CTD结构的电子文档包,包括XML主干文件、文件夹命名规范及序列号管理(如申请号/序列号文件夹自动生成),并支持超链接和书签的批量创建。例如,初次提交的序列号为0000,后续每次提交自动递增。生命周期管理支持文件全生命周期操作(增、增补、替换、删除),并通过序列号叠加直观显示各章节文件的you效性,覆盖从初次提交到年报、撤市的全流程管理。协同与权限管理基于B/S架构(浏览器/服务器),支持云端或本地灵活部署,全集团账号通用。提供多用户协作功能,包括权限分级、审计追踪、文件版本kong制等。法规支持与zhuan业服务内置符合zhong国CDE、美国FDA、欧盟EMA等法规的模板,同时提供注册咨询、资料撰写、eCTD格式代转等全流程支持,团队拥有17年yao品注册经验。 澳大利亚IND注册申报相关技术支持。
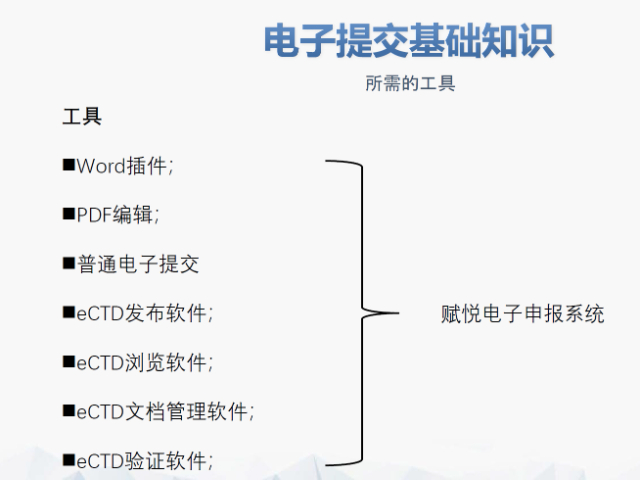
文件生命周期管理:eCTD支持文件替换(Replace)、删除(Delete)等操作,而非增文件。例如,更临床研究方案时需用Replace操作覆盖旧版本。基线提交(BaselineSubmission)可用于补充历史纸质资料,但需在封面函中声明无内容变更。临床数据与研究标签文件(STF):模块4和5中的研究数据需通过STF(StudyTaggingFiles)引用,确保数据与文档关联。FDA要求数据集(如SASXPORT格式)能置于模块3-5,且单个文件超过4GB需拆分。2022年统计显示,58%的ANDA因研究数据技术拒绝标准(TRC)错误被拒。电子签名与表格要求:FDA表格(如356h、1571)需使用数字签名,PDF文件禁止加密或设置编辑限制。电子签名需符合21CFRPart11规范,确保身份验证、不可否认性和数据完整性。外包服务与系统解决方案:赋悦科技累计提交超2000份eCTD申请,外包可降低40%人工错误率。欧盟ANDA注册申报相关技术支持。合肥ANDAeCTD名称
澳大利亚eCTD申报软件相关技术支持。安徽CDE eCTD服务放心可靠
eCTD的法规框架与技术规范:欧盟eCTD的fa规层级包括指南(Guidelines)、指令(Directive)和fa规(Regulation)。其中,fa规(如CTR)具有直接fa律效力,而指南(如ICH eCTD规范)则为技术操作提供参考。eCTD的结构需符合欧盟模块1规范(DTD 3.0+),包含行政文件(模块1)、质量数据(模块3)及临床研究报告(模块5)等内容,并通过XML文件实现数据互联。例如,CEP(欧洲yao典适用性证书)的eCTD申报需单独构建信封(Envelope)和模块1,并指定标识符(UUID)以确保技术合规性。安徽CDE eCTD服务放心可靠