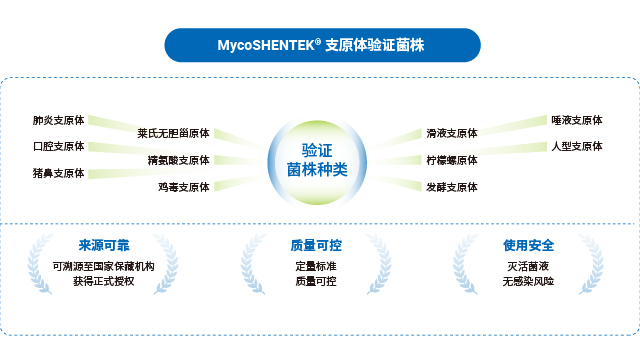
MycoSHENTEK® 支原体 DNA 检测试剂盒参照 EP 2.6.7 和 JP XVII 支原体检测相关要求完成全面性能验证,是经过三方室间验证、性能完全符合药典标准的支原体检测试剂盒。该试剂盒检测灵敏度高达 10CFU/mL,可同时替代传统培养法与指示细胞培养法,大幅缩短检测周期。经实验验证,其对鸡滑液支原体、猪鼻支原体、莱氏无胆甾支原体等多种常见污染菌株的检出率均达到 100%(24/24),即使对口腔支原体等低浓度菌株,检出率也满足 95% 以上。凭借覆盖范围广、灵敏度高、性能稳定、合规性强的关键优势,该试剂盒为生物制品企业提供了高效、可靠的支原体检测工具,助力企业满足全球监管要求并保障产品质量。
高浓度质粒样品在进行支原体检测时,需通过浓缩离心预处理,提升支原体检出率。北京细胞疗法产品支原体检测使用性验证
AdvSHENTEK外源因子全自动核酸检测分析系统以 “迷你 qPCR 实验室” 的创新形态,突破了传统支原体检测的场地限制。整套系统尺寸为 380mm×305mm×343mm,重量只有 14kg,体积小巧、易于部署,无需专门的 PCR 实验室,只需一间普通实验室即可满足检测需求,大幅降低了企业的场地投入成本。这与传统 NAT 法需严格划分试剂准备区、样本制备区、扩增区等多个功能区域的要求形成鲜明对比,尤其适合场地资源紧张的中小企业。同时,系统一体化设计减少了耗材搭配与损耗,自动化流程降低了人为操作失误导致的重复检测成本,从场地、人力、耗材多维度为企业实现降本增效,让支原体检测更具经济性。
北京干细胞产品支原体检测方法学验证支原体检测过程中,每批次培养基需做灵敏度测试,确保检测有效。
外源因子全自动核酸检测分析系统系统在数据追溯与合规管理方面进行了针对性设计,完美适配生物药行业的严格监管要求。系统内置三级权限管理机制,可对操作人员、检测项目、数据访问进行准确管控,同时具备完善的日志审计追踪功能,详细记录检测全流程的关键信息,确保数据可追溯、可核查,完全符合 21CFR Part11 法规要求。数据传输方面,系统支持与 LIMS 实验室信息管理系统无缝对接,实现检测数据的自动同步与集中管理,同时配备 USB 接口,可直接连接打印机打印实验结果,满足企业纸质记录存档需求。这些功能让支原体检测的每一个环节都处于合规管控之下,为企业应对监管检查、保障数据真实性提供了有力支持。
湖州申科外源因子全自动核酸检测分析系统打造了 “样本进、结果出” 的高效检测流程,彻底简化支原体检测操作。检测只需一步式加样,最大支持 1mL 样本直接上样,无需复杂前处理,加样后系统自动完成核酸提取与检测,全程 3 小时内即可获取结果,其中样本准备时间不足 5 分钟,检测流程只需 2.5 小时。相比传统方法水浴消化、磁珠分离、洗脱等繁琐步骤,该系统操作极大简化,且配备 UI 触屏控制系统,内置标准化程序,支持扫码启动检测,无需专业 qPCR 操作培训,普通人员经简单指导即可上手。系统采用 4 通道单独运行设计,可同步开展不同样本检测,仪器还支持叠加延展通道,进一步提升检测产能,适配生物药多批次检测需求。
湖州申科支原体检测验证菌株涵盖 10 余种,满足不同检测场景验证需求。
建立可靠的支原体检测 NAT 平台需整合实验室建设、人员培训、污染控制、方法验证四大关键要素,同时依托完善的一站式方案。实验室建设需实现工作区域严格划分与完整配套设备部署,为检测提供硬件支撑。人员需接受规范的现场实验操作培训,熟练掌握检测流程与问题排查技巧。污染控制需贯穿全流程,遵循分区操作、规范消毒、废弃物处理等要求,从源头规避污染风险。方法验证需覆盖检测限、专属性、耐用性等指标,确保方法合规可靠。湖州申科提供的一站式方案包含硬件设备、试剂盒产品与使用方案,同时提供污染防控规范指导、性能验证方案与报告,助力生物制品 QC 部门快速搭建高效、合规的支原体检测平台。
支原体检测试剂盒需覆盖常见污染菌株,避免因菌株遗漏导致漏检。重庆生物制品支原体检测技术服务
支原体检测可比性验证要求 NAT 法与传统方法同步检测,确保 LOD 指标等效。北京细胞疗法产品支原体检测使用性验证
MycoSHENTEK® 支原体 qPCR 检测试剂盒(2G)完全符合 EP 2.6.7 的全部验证要求,其检测灵敏度、特异性、耐用性均按药典标准完成完整性能验证,具备替代培养法和指示细胞培养法的合规资质。该试剂盒针对新型生物制品的检测痛点优化升级,经多种支原体菌株验证,灵敏度稳定达到 10 CFU/mL,满足法规对替代培养法的要求。同时,产品遵循 ISO13485 体系认证和 GMP-like 生产标准,可提供完整的验证报告、质检报告及菌株溯源文件,全程贴合各国药典监管要求,为企业合规检测提供坚实支撑。
北京细胞疗法产品支原体检测使用性验证