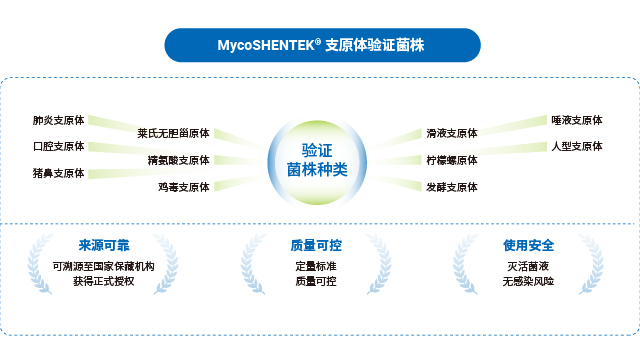
湖州申科的支原体验证菌株是支原体检测 NAT 方法验证的可靠选择,具备多重质量保障。菌株来源可靠,均取自国内外认可的合规机构验证菌株标准盘,溯源至美国模式菌种收集中心(ATCC)、中国兽医微生物菌种保藏管理中心(CVCC)等正规保藏机构,获得正式授权商用,如口腔支原体、肺炎支原体溯源至 ATCC,猪鼻支原体溯源至 CVCC。菌株生产在 BSL-2 生物安全实验室开展,符合国家生物安全法标准,针对不同菌株特性逐个优化生产工艺,涵盖超 10 种菌株的主代与工作代。质控环节严谨,采用固体平皿培养法测定 CFU(菌落形成单位),冻存前后均进行检测,确保菌落易观察分离与计数准确性;同时联合官方机构建立数字 PCR 标定方法,开展实验室间对比验证,监控 GC/CFU 比值,保障菌株活性与定量准确性,标定浓度涵盖 10CFU 和 100CFU,满足 NAT 方法验证需求。
湖州申科提供支原体检测技术培训,助力实验室提升检测能力与合规水平。重庆重组药物支原体检测使用性验证
针对新型生物制品中 10⁷细胞基质、全血、1mg/mL 高浓度质粒、5% 人白等特殊复杂样品基质,MycoSHENTEK® 支原体 qPCR 检测试剂盒(2G)进行了方法性能验证,展现出极强的样品适用性。实验数据显示,在 CHO-S&Vero 细胞(10⁷个)、5% 人血白蛋白、全血等基质中,该试剂盒对 10 CFU/mL 或 100 CFU/mL 的支原体均能稳定检出,扩增曲线清晰可靠。其优化的前处理流程与检测体系有效规避了复杂基质的干扰,无需额外传代步骤,彻底解决了传统方法在复杂样品检测中易受抑制、结果不准的问题,覆盖病毒、培养液、成品等多种样品类型。
湖南细胞疗法产品支原体检测技术服务支原体检测结果判定需结合 FAM 与 VIC 信号,警惕基质抑制导致的误判。
AdvSHENTEK 一体化支原体检测试剂盒具备较广的检测覆盖范围与极强的专属性,能应对各类潜在污染风险。试剂盒可准确检出近 200 种微生物,包括支原体、螺原体、无胆甾原体、虫原体及中间原体,覆盖生物药生产中常见的污染菌株类型。经严格验证,对鸡滑支原体、精氨酸支原体、猪鼻支原体、肺炎支原体等多种菌株,在 10CFU/mL 和 100CFU/mL 浓度下的阳性检出率均达到 24/24,其中包含多个 ATCC 标准菌株。同时,试剂盒专属性强,无交叉干扰现象,能有效区分目标菌株与其他非目标微生物,避免假阳性结果,确保检测数据的准确性,为企业排查支原体污染提供可靠保障。
AdvSHENTEK外源因子全自动核酸检测分析系统凭借优越性能,为支原体检测提供坚实技术支撑。硬件方面,系统温度运行精度≤0.5℃,温度波动控制在 ±0.5℃以内,荧光强度 CV≤3%,确保检测结果的重复性与准确性;4 通道单独运行且支持同步检测,通道可叠加延展,兼顾检测效率与灵活性。软件方面,系统具备三级权限管理、日志审计追踪功能,完全符合 21CFR Part11 法规要求,支持 LIMS 系统连接、USB 数据导出及打印机直接打印,满足企业合规追溯需求。此外,系统运输与储存便捷,仪器可常规运输,检测试剂盒在 2-8℃环境下即可稳定保存,无需特殊冷链条件,进一步提升了产品的实用性与适配性。
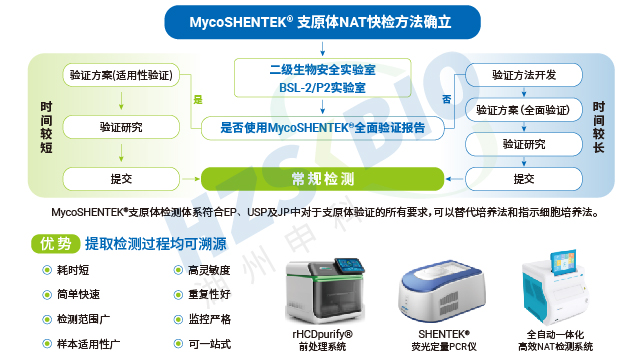
支原体检测 NAT 法验证报告需包含检测限、专属性、耐用性等完整数据。
取样量的科学设计直接影响支原体检测的代表性与灵敏度,需结合样品总体积、基质特性综合考量。法规建议:产品总体积大于1000mL的按无菌检查法取样,10-1000mL 取总体积的 1%,1-10mL 取 100μL,小于1mL的需采用替代取样方案。实际检测中,取样体积越大,灵敏度越高,但需平衡洗脱液消耗与重复检测需求。此外,支原体兼具胞内胞外生存特性,只检测上清会导致漏检,需采用细胞裂解等处理方式,确保覆盖全部污染靶点,提升检测结果的真实性。
病毒收获液、抗体 UPB 等中间产物需逐批检测支原体,把控生产过程质量。重庆重组药物支原体检测使用性验证
湖州申科支原体检测试剂盒通过FDA DMF备案,支持全球药品申报使用。重庆重组药物支原体检测使用性验证
湖州申科外源因子全自动核酸检测分析系统打造了 “样本进、结果出” 的高效检测流程,彻底简化支原体检测操作。检测只需一步式加样,最大支持 1mL 样本直接上样,无需复杂前处理,加样后系统自动完成核酸提取与检测,全程 3 小时内即可获取结果,其中样本准备时间不足 5 分钟,检测流程只需 2.5 小时。相比传统方法水浴消化、磁珠分离、洗脱等繁琐步骤,该系统操作极大简化,且配备 UI 触屏控制系统,内置标准化程序,支持扫码启动检测,无需专业 qPCR 操作培训,普通人员经简单指导即可上手。系统采用 4 通道单独运行设计,可同步开展不同样本检测,仪器还支持叠加延展通道,进一步提升检测产能,适配生物药多批次检测需求。
重庆重组药物支原体检测使用性验证