- 产地
- 苏州
- 品牌
- 细胞外基质胶
- 型号
- 齐全
- 是否定制
- 是
细胞外基质与医学:恶性部位的发生、发展、侵袭和转移常常伴有细胞外基质(extracellularmatrix,ECM)及其细胞表面受体表达的变化。正常肝细胞没有基膜,也不表达层粘连蛋白(laminin,LN)的特异性整合素族受体α6β1;而在肝细胞(humanhepatocellularcarcinoma,HCC)组织中,LN和α6β1不仅表达水平升高,呈明显的共分布,而且其高水平表达与肝患者的预后呈负相关,提示HCC细胞可能通过α6β1受体接受来自LN的信号,从而对肝细胞的侵袭行为起着不可忽视的作用。肝的发病过程中往往早期就出现门静脉侵袭、肝内转移以及肝外肺脏和骨组织的转移,肝的侵袭、转移和术后复发是影响患者预后的主要因素。基质金属蛋白酶(matrixmeta-lloproteinases,MMPs)对ECM的降解是部位细胞侵袭和转移的关键环节之一,多种恶性部位都伴有MMPs分泌水平和活性的增高。纤连蛋白与细胞外结构域的连接启动细胞内信号通路,并通过一组衔接分子如肌动蛋白与细胞骨架结合。长沙正规细胞外基质胶厂家直销

基质:曾称为“一种分析物(analyte)的环境(milieu)”,即指标本中除分析物以外的一切组成。以血清胆固醇(Chol)测定而言,就是指Chol以外血清中的一切成分及其物理、化学性质。基质是由生物大分子构成的无定形胶状物,无色透明,具有一定黏性,孔隙中有组织液。细胞外基质的物理性质主要受细胞外基质中蛋白聚糖所携带的多糖基团的影响,蛋白聚糖是由糖胺聚糖以共价的形式同线性多肽连接而成的多糖和蛋白复合物。另外一种基质是植物栽培用的一种人工土壤。上海正规细胞外基质胶直销厂家由于其不同的性质和组成,细胞外基质可以发挥许多功能。
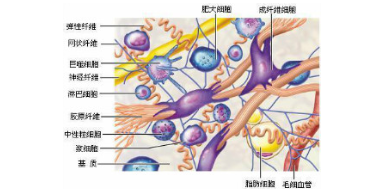
细胞外基质的主要类型及功能:对人类细胞的研究表明,细胞外基质中的纤粘蛋白主要由成纤维细胞、上皮细胞等分泌并附着在细胞表面,其作用是促进细胞对基质的贴附,细胞之间的粘着,细胞内微丝及应力纤维的构建。观察到转化的体外培养的成纤维细胞,表面纤维蛋白量减少,与此相关地细胞形态变圆,与培养基底贴附松弛,胞内应力纤维很大减少,细胞密集,重叠生长。这种转化细胞接种入正常机体,常能长成块,并侵润正常组织,发生普遍转移。又如上皮细胞分泌胶原蛋白和膜粘蛋白于上皮组织的基底层上,反之,这些蛋白又作为信号“指挥”上皮细胞生长、迁移的方向。在胚胎发育或愈伤再生时,上皮细胞正是沿着基底层发展的。由此可知,调节细胞生长、发育的若干信息正是通过胞外基质传递的。
免疫系统和细胞外基质之间的串扰:被囊动物是脊索动物中的尾索动物,成年海鞘包被着由被膜组成的细胞外基质。伤口愈合过程中,被膜基质被免疫细胞重塑,如脱粒细胞。细菌与海鞘之间的相互联系已有报道,可能涉及分泌活性产物,如克菌蛋白与吞噬细胞一起作为先天免疫系统的一部分。在棘皮动物中,造血组织被描述为分泌体腔细胞的体腔上皮,这些是伤口愈合的重要调节剂,因为它们迁移到伤口部位形成血块,并在ECM的调节中发挥作用。在海参中体腔细胞可能是免疫反应和伤口修复的重要调节器。细胞外基质对细胞的基本生命活动发挥很全的生物学作用。

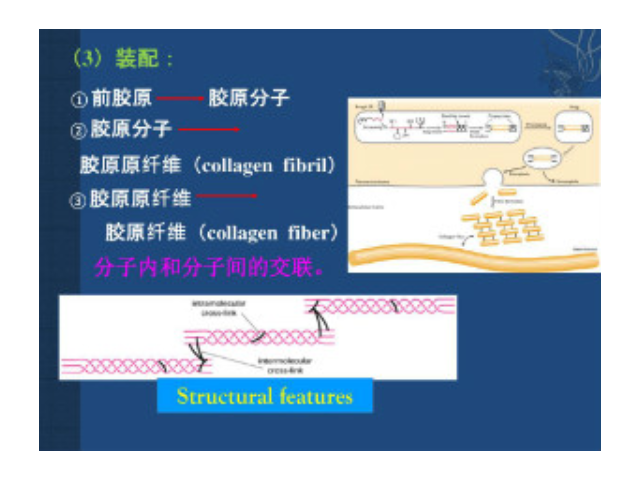
蛋白聚糖在细胞外基质中的功能是什么:。单个的蛋白聚糖和透明质酸-蛋白聚糖复合物直接与胶原纤维连接形成动物细胞外的纤维-网络(fiber-network)结构,不同类型的胶原和不同类型的蛋白聚糖连接形成不同的纤维-网络,对于提高细胞外基质的连贯性起关键作用。此外,蛋白聚糖还可作为细胞粘着的暂时性或长久性的位点。暂时性的粘着发生在胚胎发育中,对于单个细胞及细胞层的移动具有重要作用。另外,蛋白聚糖对于细胞分化也十分重要,同时也与细胞有关细胞外基质的生物学作用:调节细胞的增殖。长沙正规细胞外基质胶厂家直销
绝大多数哺乳类动物细胞之间存在成分复杂的细胞外基质(ECM)。长沙正规细胞外基质胶厂家直销
细胞外基质:为了获得体内衍生的仿生基质,从心脏末端抽取全血,离心后取上层血液与预提取的EVs混合,进行自凝集。通过压缩将自凝混合物制备成一定形状的血源性水凝胶(AH)。通过SEM观察发现EVs附着在纤维上,因而说明AH与Evs可成功结合(图3A,B)。检测ALP活性和钙浓度发现两者都随时间增加,持续到AH降解完毕,说明含EV的AH具有缓慢、渐进的释放特性(图3C,D)。然后建立共培养体系,比较AH、AH+E-EVs、AH+L-EVs、AH+C-EVs(AH与E-EVs、L-EVs复合)对BMSCs活力、增殖、迁移、成骨分化的影响(图3E-K),结果表明AH与E-EVs具有协同作用,可促进BMSCs的增殖和迁移,并且AH与E-Evs的联合应用可以促进早期骨形成。长沙正规细胞外基质胶厂家直销
细胞外基质:为了获得体内衍生的仿生基质,从心脏末端抽取全血,离心后取上层血液与预提取的EVs混合,进行自凝集。通过压缩将自凝混合物制备成一定形状的血源性水凝胶(AH)。通过SEM观察发现EVs附着在纤维上,因而说明AH与Evs可成功结合(图3A,B)。检测ALP活性和钙浓度发现两者都随时间增加,持续到AH降解完毕,说明含EV的AH具有缓慢、渐进的释放特性(图3C,D)。然后建立共培养体系,比较AH、AH+E-EVs、AH+L-EVs、AH+C-EVs(AH与E-EVs、L-EVs复合)对BMSCs活力、增殖、迁移、成骨分化的影响(图3E-K),结果表明AH与E-EVs具有协同作用,可促进BMS...
- 上海成都细胞外基质胶 2026-03-23
- 贵阳正规细胞外基质胶服务电话 2026-03-23
- 珠海正规细胞外基质胶哪家好 2026-03-23
- 芜湖正规细胞外基质胶哪家好 2026-03-23
- 唐山细胞外基质胶厂家推荐 2026-03-23
- 太原正规细胞外基质胶哪里买 2026-03-23
- 开封正规细胞外基质胶直销厂家 2026-03-23
- 长沙正规细胞外基质胶厂家直销 2026-03-22
- 开封正规细胞外基质胶平均价格 2026-03-22
- 无锡细胞外基质胶平均价格 2026-03-22
- 太原细胞外基质胶单价 2026-03-22
- 天津正规细胞外基质胶厂家 2026-03-21
- 太原细胞外基质胶服务电话 2026-03-21
- 苏州细胞外基质胶厂家推荐 2026-03-21
- 广州正规细胞外基质胶哪家好 2026-03-21
- 徐州细胞外基质胶产品介绍 2026-03-21


- 徐州唐山RNA提取试剂 03-23
- 珠海原代细胞分离试剂盒单价 03-23
- 合肥开封RNA提取试剂 03-23
- 贵阳正规细胞外基质胶服务电话 03-23
- 珠海正规细胞外基质胶哪家好 03-23
- 杭州正规外泌体提取试剂 03-23
- 徐州正规外泌体提取试剂 03-23
- 芜湖正规细胞外基质胶哪家好 03-23
- 温州正规RNA提取试剂供应商 03-23
- 芜湖RNA提取试剂直销价 03-23